
 |
|
|
Главная Переработка нефти и газа 50 то 150 200 250 300 Ш TeMnepamijpa , °С Рис. III.7. Вязкость метана (в мкПа-с) в зависимости от давления и теипературы. 0 30 20 10
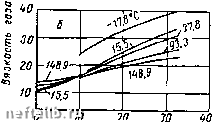 Давление, ИПа Рис. III.8. Зависимость вязкости газов (в мкПа-с) различной плотности от давления и температуры. Плотность газа р: о - 0,6; 6 - 0,7-в - 0.8; г - 0,9; д - 1,0. 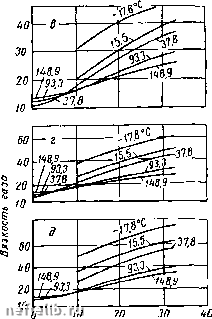 Давление, ППа л о 5 Ю 15 го 25 Давление, una Рис. III.9. Зависимость вязкости азота (в мкПа -с) от давления и температуры. различных давлениях и температурах обычно определяют по экспериментальным данным. При небольших величинах давления и температур растворимость газов в нефти практически подчиняется закону Генри - количество газа Vj., растворенного при данной температуре в единице объема V. жидкости, пропорционально давлению р газа над поверхностью Vj = apV, (П1.58) где а - коэффициент растворимости газа. [a] = -j3- или [а]: Н мЗ-{кгс/см2) Из (П1.59) следует, что коэффициентом растворимости учитывается количество газа, растворяющегося в единице объема жидкости при увеличении давления на единицу. Коэффициент растворимости реальных газов не является постоянной величиной и зависит от рода жидкости и газа, от давления, температуры и от других факторов, которые приобретает раствор газа в жидкости. Это связано с общим отклонением реальных газов от идеального газа. Как уже упоминалось, введение понятия летучести (фугитивности) / позволяет связать найденные опытным путем свойства реального газа с его термодинамическими параметрами (т. е. подстановка вместо давления летучести / в формулы, основанные на идеализированном представлении о процессе, позволяет использовать их для описания реальных процессов). Как известно, метод этот распространяется и на растворы. Используем далее понятие летучести при рассмотрении вначале растворимости однокомпонентных газов в жидкостях. При исследовании теоретических вопросов растворимости газов закон Генри обычно записывается через мольные концентрации газа в растворе N = ap p = ±N-aN, (1П.60) где N - мольная концентрация газа в растворе. Здесь и Пр - число молей жидкой и газовой фаз в системе. Тогда, с учетом летучести закон Генри запишется в виде \im-L = a{p,T). (П1.61) Уравнение (III.61) можно применять лишь нри концентрациях газа, приближающихся к нулю. Получение зависимостей концентрации газа в жидкости от давления затрудняется не только вследствие отклонения реальных газов от законов идеального, но также и потому, что в растворе реальный газ приобретает специфические свойства. Внешним выражением этих свойств является увеличение объема раствора нри введении в него газа. Повышение объема влияет на концентрацию газа в жидкости. Приращение объема раствора определяется количеством растворенного газа, свойствами жидкости и газа, температурой и давлением. Увеличение объема жидкости обычно характеризуют величиной представляющей собой приращение объема жидкости нри растворении в ней 1 кг газа. Эту величину V называют кажущимся удельным объемом растворенного газа в жидкой фазе. ~ G Смысл понятия «кажущийся» заключается в том, что приращение-объема А V жидкости (нефти) не представляет собой истинного объема растворенного газа в нефти, а является результатом взаимодействия молекулярных сил растворенного газа и жидкости. В химической термодинамике величину Указывают парциальным мольным объемом. С учетом отклонения законов реальных газов от законов идеального, а также изменения объема раствора нри введении в него газа И. Р. Кричевским дается следующее уравнение, связывающее концентрацию газа в жидкости с давлением In-L = ln.L+FiPz, (П1.62) где / - летучесть газа в газовой фазе; N - мольная концентрация газа в растворе; р - общее давление над раствором; Ро - упругость пара растворителя; /о - летучесть газа нри давлении, равном упругости пара растворителя при температуре Т\ Nf, - мольная концентрация газа в растворе при давлении ро; V - кажущийся (парциальный) мольный объем. Из (III.62) получим гЯо 1 fo V (P-Pt) /. (П1.63) Из (III.63) следует, что зависимость коэффициента растворимости от давления и температуры определяется соотношением " = 4г-уткг> ("1-64) т. е. коэффициент а с увеличением давления уменьшается. 0 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 [ 30 ] 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 56 57 58 59 60 61 62 63 64 65 66 67 68 69 70 71 72 73 74 75 76 77 78 79 80 81 82 83 84 85 86 87 88 89 90 91 92 93 94 95 96 97 98 99 100 |
||||||||||||||||||||||||||||||||||||||
 |
 |