
 |
|
|
Главная Переработка нефти и газа исходные компоненты (рис. 53, а); в то же время они сохраняют достаточно высокую пластичность. Твердые растворы из-за сочетания повышенной прочности и хорошей пластичности выгодно использовать как основу для конструкционных сплавов. Образование твердых растворов сопровождается значительным увеличением электрического сопротивления, что связано с сильным искажением электрического поля металла-растворителя атомами растворенного компонента и уменьшением температурного коэффициента электросопротивления. Поэтому твердые растворы применяют для изготовления проволоки (ленты), используемой в электронагревательных элементах и реостатах. В сплавах с ограниченной растворимостью свойства при концентрациях, отвечающих однофазному твердому раствору, изменяются по криволинейной зависнмостп (рис. 53, б). В области механической смеси двух фаз а и р свойства изменяются по прямой, т. е. представляют собой среднее из свойств фаз, образующих смесь. Так, если одна фаза мягкая и пластичная, а другая твердая и хрупкая, то сплав тем тверже и хрупче, чем больше в нем второй фазы. При концентрации, соответствующей химическому соединению (рис. 53, е), наблюдается характерный перелом кривой свойств (сингулярная точка). Это объясняется тем, что свойства химических соединений отличаются от свойств образующих их компонентов. Химические соединения, особенно соединения металла с углеродом (карбиды) и азотом (нитриды), имеют очень высокую твердость, но хрупки. Указанные схемы дают приближенную зависимость свойств от состава и строения сплава. Свойства сильно зависят от тонкого строения сплава (размера блоков, искажений кристаллической решетки), величины зерна, степени дисперсности фаз и т. д. А. А. Бочвар показал, что существует определенная связь мовду типом диаграммы состояния и литейными свойствами. Сплавы - твердые растворы-имеют низкие литейные свойства (плохая жидкотекучесть g, склонность к образованию рассеянной пористости У„ и трещинам). Для получения высоких литейных свойств концентрация компонентов в литейных сплавах должна превышать их максимальную растворимость в твердом со- стоянии и приближаться к эвтектическому составу. Эвтектические сплавы обладают хорошей жидкотеку-честьго, и усадка в них проявляется в виде сконцентрированной раковины. Сплавы, лежащие левее точки а (предельной растворимости в твердом растворе) и состоящие в основном из а-фазы, пластичны, и поэтому хорошо прокатываются, куются, прессуются и т. д. (рис. 53, б). Пластичность сильно снижается при появлении в структуре эвтектики. Поэтому в деформируемых сплавах максимум растворимости при эвтектической температуре (рис. 53, б, точка а) является верхним желательньш пределом содержания компонентов. Глава ЖЕЛЕЗО И ЕГО СПЛАВЫ VIII I, Диаграмма состояния железо-углерод Сплавы железа распространены в промышленности наиболее широко. Главные из них - сталь и чугун - представляют собой сплавы железа с углеродом. Для получения заданных свойств в сталь и чугун вводят легирующие элементы. Ниже будет рассмотрено строение и фазовые превра-ш,ення в сплавах железо-углерод, а такх<е фазы в СП .авах железа с легирующими элементами. Компоненты и фазы в системе железо-углерод Чистое железо - металл серебристого цвета. Температура плавления железа 1539 °С. Чистое железо, которое может быть получено в настоящее время, содержит 99,999 % Fe. Технические сорта железа содержат 99,8-99,9 % Fe. Железо известно в двух полиморфных модификациях а и V- Модификация а-железо (Fe„) существует при температурах ниже 910 °С и выше 1392 С (рис. 54). Для интервала температур 1392-1539 "С а-железо нередко обозначают как 6-железо (Fe). Кристаллическая решетка а-железа - объемноцен-трированный куб с периодом решетки а == 0,28606 нм (рис. 54). До температуры 768 °С железо магнитно (ферромагнитно). Критическую точку (768 °С), соответствующую магнитному превращению, т. е. переходу из ферромагнитного состояния в парамагнитное, называют точкой Кюри и обозначают (рис. 54). то то гец-FEy -Магиипное пребращение \9tt4h) тЧк) 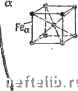 Рис. 54. Кривая охлаждения железа -у-Железо (Fe.(,) существует при температуре 910- 1392 °С; оно парамагнитно. Критическую точку у «-превращения при 910 "С обозначают соответственно Ас (при нагреве) и Аг. (прн охлаждении). Критическую точку перехода железа при 1392 °С обозначают Ас (при нагреве) и Аг (при охлаждении). Кристаллическая решетка -елеза - гранецен-трированный куб (рис. 54) с периодом решетки а ~ = 3,645 нм при температуре 910 °С. 0 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 [ 27 ] 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 56 57 58 59 60 61 62 63 64 65 66 67 68 69 70 71 72 73 74 75 76 77 78 79 80 81 82 83 84 85 86 87 88 89 90 91 92 93 94 95 96 97 98 99 100 101 102 103 |
||
 |
 |